1.4:OCTAVAS DE NEWLANDS(1864)
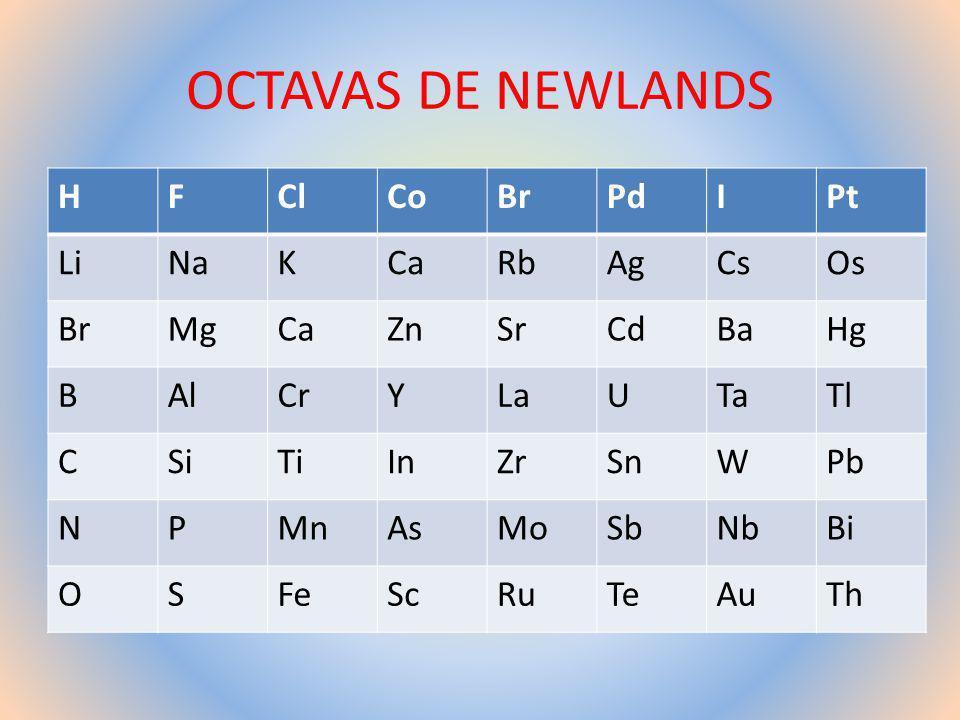
En 1865, el químico inglés John Alexander Reina Newlands, intentó solucionar el problema del comportamiento periódico de los elementos, colocando los elementos más ligeros en orden creciente según sus pesos atómicosNewlands se dio cuenta que el octavo elemento se asemejaba al primero, así como el noveno era similar al segundo, etc. A esta observación se le llama, “Ley de las octavas de Newland”, en honor al químico inglés.
Como cada ocho elementos, aparecía otro elemento de iguales propiedades, a Newlands se le ocurrió hacer la comparación entre sus octavas, con las octavas musicales, observando que la periodicidad de las octavas químicas, sugería una armonía como si de música se tratase. Dicha comparación, a pesar de ser idílica y atractiva, carecía de validez alguna, pero fue por ella que a su clasificación le dio el nombre de Octavas de Newlands.
Posteriormente se descubrió una familia de compuestos inertes, formada por el helio, neón, argón, kriptón, y xenón, o lo que es lo mismo, el grupo de los gases nobles. Este descubrimiento transformó a las octavas de Newlands, en novanas.
Los esfuerzos de Newlands, supusieron un gran paso con buena dirección, en los que a clasificación de elementos se refería pero, sin embargo, pueden destacarse tres grandes críticas a su esquema clasificatorio:
- No existía un lugar indicado para los elementos recientemente descubiertos.
- No tuvo mucha consideración con los pesos atómicos, ni siquiera realizó una estimación aproximativa de los valores más probables.
- Algunos elementos no encajaban en el esquema de Newlands , como por ejemplo , el cromo, que quedaba mal posicionado bajo el aluminio, y el magnesio, que es un metal, venía colocado bajo el fósforo que es un no metal, así como el hierro que tratándose de un metal, se encontraba debajo del azufre (no metálico), así que tanto éstos, como otros elementos, no encajaban de ninguna manera en el esquema.